Uit een groot nieuw onderzoek is gebleken dat de genen die we bij onze geboorte erven, een veel belangrijkere rol spelen bij kanker dan tot nu toe werd gedacht. Ze beïnvloeden niet alleen hoe tumoren ontstaan en groeien, maar ook hoe ze reageren op behandelingen.
In tegenstelling tot het meeste kankeronderzoek, dat zich richt op mutaties die gedurende een heel leven worden opgelopen, onderzocht deze studie miljoenen genetische varianten en hun effecten op de eiwitactiviteit in tumoren. Deze bevindingen kunnen de manier waarop we kanker diagnosticeren en behandelen veranderen, doordat we rekening houden met de unieke genetische achtergrond van iedereen, en niet alleen met de mutaties in de tumor. Dit is een stap in de richting van echt gepersonaliseerde, uitgebreide kankerzorg.
Genetica en de mogelijke effecten van kanker
Uit een nieuw internationaal onderzoek onder leiding van onderzoekers van de Icahn School of Medicine op Mount Sinai, in samenwerking met het Clinical Tumor Proteomics Consortium (CPTAC) van het National Cancer Institute, is gebleken dat de genen die we bij onze geboorte erven, de zogenaamde kiemlijngenetische varianten, een veel belangrijkere rol spelen bij kanker dan voorheen werd gedacht.
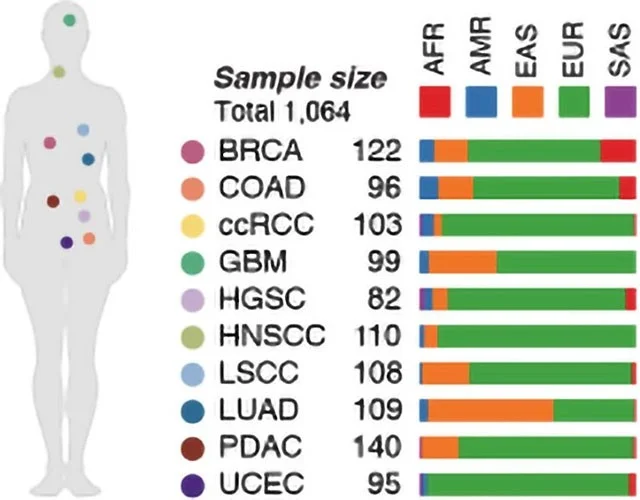
Dit is de eerste studie die laat zien hoe miljoenen erfelijke genetische verschillen de activiteit van duizenden eiwitten in tumoren kunnen beïnvloeden. Door gegevens van meer dan 1.000 patiënten met 10 verschillende soorten kanker te analyseren, ontdekten onderzoekers dat het erfelijke DNA van een persoon invloed kan hebben op de manier waarop kanker zich in zijn of haar lichaam ontwikkelt.
Deze inzichten kunnen de manier waarop kanker wordt behandeld veranderen. Momenteel worden de meeste behandelingen bepaald door genetische mutaties die in de tumor zelf worden aangetroffen. Uit dit onderzoek blijkt dat er betere mogelijkheden zijn om kanker te diagnosticeren, het risico hierop te beoordelen en behandelopties te kiezen als er meer rekening wordt gehouden met de erfelijke genetische achtergrond van de patiënt.
" Iedereen draagt vanaf de geboorte een unieke combinatie van genetische variaties met zich mee, en deze genetische verschillen bepalen in stilte hoe onze cellen gedurende ons hele leven functioneren ", aldus medeauteur van de studie Zeynep H. Gümüş, PhD, universitair hoofddocent genetica en genoomwetenschappen aan de Icahn School of Medicine. Deze genetische inzichten kunnen een actieve rol spelen in hoe tumoren ontstaan, hoe ze groeien en zelfs hoe ze reageren op behandeling. Dit opent nieuwe mogelijkheden om kankerzorg af te stemmen, niet alleen op de tumor zelf, maar ook op de onderliggende genetische samenstelling van een patiënt .
Van somatische mutaties tot genetische variatie
Tot op heden richt het kankeronderzoek zich vooral op somatische mutaties: veranderingen die gedurende het leven van een persoon in cellen optreden. Maar er zijn veel meer genetische varianten in de kiemlijn dan somatische mutaties, en hun invloed op kanker is nog niet goed begrepen.
Om het onderzoek uit te voeren, maakten de onderzoekers gebruik van een geavanceerde techniek genaamd precisiepeptidomics. Daarmee konden ze onderzoeken hoe specifieke genetische mutaties de structuur, stabiliteit en functie van eiwitten in kankercellen moduleren. Door meer dan 330.000 eiwitcoderende genetische varianten in kaart te brengen, ontdekte het team hoe deze genetische verschillen de eiwitactiviteit kunnen veranderen, de genexpressie kunnen beïnvloeden en zelfs de manier kunnen bepalen waarop tumoren interacteren met het immuunsysteem.
Uit het onderzoek blijkt dat erfelijke veranderingen in het DNA invloed kunnen hebben op de manier waarop genen tot expressie komen en hoe eiwitten – belangrijke factoren die kankergedrag aanjagen – in tumoren worden geproduceerd en gereguleerd. Deze variaties helpen een deel van de grote verschillen te verklaren die artsen zien in de manier waarop kanker ontstaat, zich ontwikkelt en reageert op verschillende behandelingen.
Dit onderzoek bevestigt het groeiende bewijs dat gepersonaliseerde kankerbehandelingen niet alleen rekening moeten houden met de mutaties in de tumor, maar ook met de genetische achtergrond van de persoon. De onderzoekers waarschuwen echter dat de bevindingen van het onderzoek gebaseerd zijn op gegevens van een groep patiënten van voornamelijk Europese afkomst. Er is meer onderzoek nodig om ervoor te zorgen dat deze inzichten ook van toepassing zijn op multi-etnische populaties.